公共衛(wèi)生學院郝燕霞及其合作者在Neurotoxicity Research發(fā)文報道鋁誘導小鼠腦組織“混合”細胞死亡和潛在的干預方式,。
2019年10月4日,在Neurotoxicity Research(《神經(jīng)毒性研究》)以“Aluminum-induced “mixed” cell death in mice cerebral tissueand potential intervention(鋁誘導小鼠腦組織“混合”細胞死亡和潛在的干預方式)”為題,,在線發(fā)表了山西醫(yī)科大學公共衛(wèi)生學院郝燕霞及其合作者的關于鋁導致小鼠腦組織發(fā)生凋亡和程序性壞死及其干預方式的新認識,。
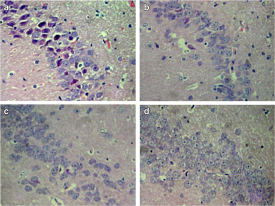
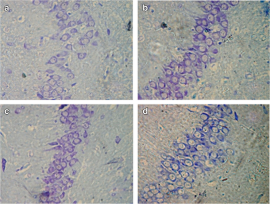
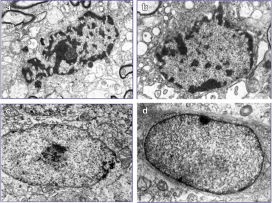
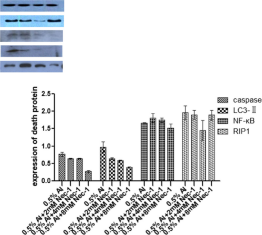
大腦是易受鋁損害的器官之一,。鋁的毒性與神經(jīng)行為缺陷、神經(jīng)細胞功能障礙和死亡有關,。本研究的目的是:1.評價細胞死亡抑制劑nec1和泛caspase抑制劑Z-VAD-FMK對鋁誘導的神經(jīng)行為缺陷和神經(jīng)元細胞死亡的修復效果,,以證明鋁誘導細胞死亡的能力。2.初步探討鋁致癡呆動物模型中使用nec1和Z-VAD治療阿爾茨海默病等神經(jīng)元細胞丟失相關疾病的可能性,。我們發(fā)現(xiàn)nec1和Z-VAD-FMK單獨或聯(lián)合使用可以減少鋁誘導的小鼠學習和記憶障礙,。病理組織學結果顯示,nec1,、Z-VAD-FMK可減少al誘導的神經(jīng)元死亡細胞,。此外,在鋁暴露小鼠大腦中,,nec1和Z-VAD-FMK可抑制細胞死亡信號通路中的一些細胞死亡相關蛋白,。結論:nec1、Z-VAD-FMK可修復鋁誘導的小鼠學習記憶損傷,。與Z-VAD-FMK相比,,nec1對學習記憶功能損傷的修復作用更明顯。nec1,、Z-VAD-FMK可修復鋁誘導的細胞形態(tài)學損傷,,減少死亡細胞數(shù)量,,且劑量越大修復效果越顯著。nec1的作用強于Z-VAD-FMK,,但作用機制不同,。他們的結合產(chǎn)生了最強的效果。我們的研究證實了al誘導的神經(jīng)細胞壞死和凋亡在動物模型中存在,,并提示了nec1和Z-VAD-FMK對神經(jīng)退行性疾病中神經(jīng)元死亡的潛在治療作用,。
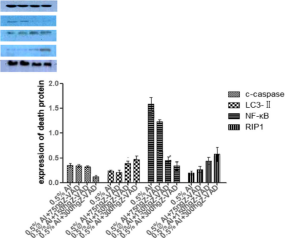
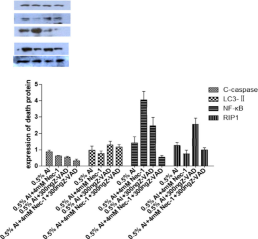
公共衛(wèi)生學院牛僑教授為本文的通信作者,公共衛(wèi)生學院2017級博士研究生郝燕霞為本論文的第一作者,。該研究得到國家自然科學基金委重點項目(81320078)資助,。

